Údar:
Lewis Jackson
Dáta An Chruthaithe:
5 Bealtaine 2021
An Dáta Nuashonraithe:
1 Iúil 2024

Ábhar
Is é Mol an t-aonad caighdeánach tomhais sa cheimic, a úsáidtear chun breathnú ar na heilimintí éagsúla i gcomhdhúil. De ghnáth, ríomhtar mais chumaisc i ngraim (g) agus is gá í a thiontú go haonaid molar. Tá an t-aistriú simplí go leor, áfach, tá roinnt céimeanna tábhachtacha ann a chaithfimid a leanúint. Agus an modh thíos á úsáid agat, is féidir leat gram a thiontú go móil.
Céimeanna
Cuid 1 de 2: Ríomh mais mhóilíneach
Ullmhaigh na soláthairtí riachtanacha chun fadhb na matamaitice a réiteach. Nuair a bheidh na huirlisí uile ar fáil agat, beidh sé níos éasca an fhadhb a réiteach. Is é atá uait:
- Peann luaidhe agus páipéar. Éiríonn an mhatamaitic níos éasca nuair a scríobhann tú gach rud ar pháipéar. Ní mór duit na céimeanna go léir a chur i láthair d’fhonn an scór uasta a bhaint amach.
- Tábla tréimhsiúil eilimintí ceimiceacha: a úsáidtear chun mais-adamh na ndúl a chinneadh.
- Áireamhán póca: úsáidtear chun uimhreacha casta a ríomh.

Faigh amach cé na heilimintí atá sa chomhdhúil a chaithfidh tú a thiontú go haonaid mholar. Is é an chéad chéim chun mais mhóilíneach a ríomh ná na heilimintí atá sa chomhdhúil a chinneadh. Tá sé seo éasca toisc nach bhfuil sa ghiorrúchán d’eilimintí ach carachtar amháin nó dhó.- Má dhéantar substaint a ghiorrú le dhá litir, déanfar an chéad litir a chaipitliú agus tá an dara litir i litreacha beaga. Sampla: Is é Mg an giorrúchán don mhaignéisiam eiliminte.
- Comhdhúile NaHCO3 tá ceithre ghné ann: sóidiam (Na), hidrigin (H), carbón (C) agus ocsaigin (O).
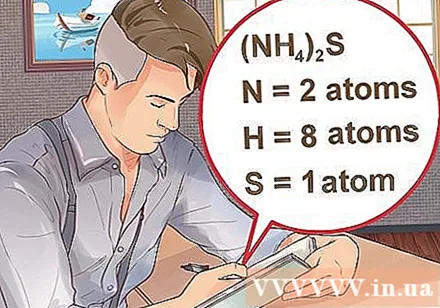
Faigh líon na n-adamh do gach eilimint sa chomhdhúil. Ní mór duit uimhir adamhach gach substainte i gcomhdhúil a bheith ar eolas agat chun mais mhóilín an chomhdhúil sin a ríomh. Léiríonn an líon beag in aice le giorrúchán na dúile uimhir adamhach na dúile.- Sampla: cumaisc H.2Tá dhá adamh hidrigine agus adamh ocsaigine amháin ag O.
- Má scríobhtar comhdhúil i lúibíní, agus innéacs beag ina dhiaidh sin, iolraíonn gach comhábhar i lúibíní an t-innéacs. Sampla: cumaisc (NH4)2Tá S comhdhéanta de dhá adamh N, ocht n-adamh H agus adamh S amháin.

Scríobh síos an páipéar adamhach ciúbach do gach eilimint. Is é an tábla peiriadach an bealach is éasca chun adamh ciúbach eilimint a fháil. Tar éis duit an eilimint a aimsiú ar an tábla peiriadach, feicfidh tú an mhais adamhach díreach faoi dheilbhín na dúile.- Mar shampla, is é 15.99 an t-adamh ciúbach ocsaigine.
Ríomh an mhais mhóilíneach. Tá mais-mhóilín substainte cothrom le líon na n-adamh de gach eilimint arna iolrú faoi mhais-adamh na dúile sin. Tá an chainníocht seo riachtanach ó thiontú gram go molar.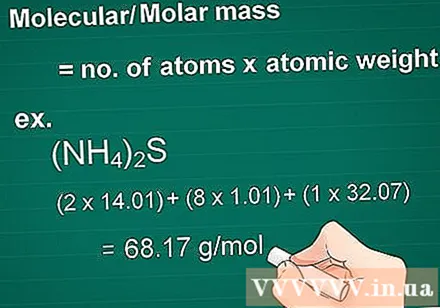
- Ar dtús, iolraigh uimhir adamhach gach eilimint sa chomhdhúil faoina mais adamh.
- Ansin, cuir maiseanna na n-eilimintí sa chomhdhúil le chéile.
- Sampla: Mais mhóilíneach comhdhúil (NH4)2S = (2 x 14.01) + (8 x 1.01) + (1 x 32.07) = 68.17 g / mol.
- Tugtar mais mhóilíneach ar mhais mhóilíneach freisin.
Cuid 2 de 2: Tiontaigh gram go mol
Socraigh an fhoirmle tiontaithe. Chun líon móil an chomhdhúil a fháil, roinn líon gram an chomhdhúil le mais molar an chomhdhúil sin.
- Foirmle: líon na mól = mais (gram) / mais molar an chomhdhúil (gram / mol)
Cuir na huimhreacha san fhoirmle. Tar éis duit an fhoirmle cheart a chur ar bun, is é an chéad chéim eile an fhoirmle a chur in ionad na n-uimhreacha a ríomh tú. Más mian leat a chinntiú go bhfuil na sonraí sa suíomh ceart, is féidir leat iad a sheiceáil tríd an aonad a chur faoi chois. Más móin an t-aonad atá fágtha tar éis na simplíochta, socraítear i gceart tú.
Réitigh an chothromóid. Ag baint úsáide as áireamhán, roinn an mhais le móilín ciúbach na substainte nó an chomhdhúil. Is é an comhrann an líon mól den tsubstaint nó den chomhdhúil atá á lorg agat.
- Mar shampla, is í an fhadhb atá ann ná 2 g uisce (H.2O) agus iarr ort é a thiontú go haonaid mholar. Tá mais molar H againn2Is é O 18g / mol. Roinn 2 faoi 18, ionas go mbeidh 0.1111 mol H2O agat.
Comhairle
- Ná déan dearmad an eilimint nó an t-ainm cumaisc a áireamh leis na freagraí.
- Má iarrtar ort cleachtadh nó tráth na gceist a chur i láthair, déan cinnte go dtaispeánann tú do chuid freagraí go soiléir trí bhosca a chur timpeall nó a tharraingt timpeall na bhfreagraí.
Cad atá uait
- Tábla tréimhsiúil ceimiceach
- Peann luaidhe
- Páipéar
- Ríomhaire
- Fadhbanna ceimice