Údar:
Christy White
Dáta An Chruthaithe:
8 Bealtaine 2021
An Dáta Nuashonraithe:
1 Iúil 2024

Ábhar
- Chun céim
- Modh 1 de 3: Cuid a hAon: Sliogáin Leictreon a Thuiscint
- Modh 2 de 3: Cuid a Dó: Leictreoin Valence a Aimsiú i Miotail, Seachas Miotail Trasdula
- Modh 3 de 3: Cuid a Trí: Leictreoin Valence a Aimsiú i Miotail Trasdula
- Leideanna
- Riachtanais
Tá leictreoin faoisimh suite i mblaosc seachtrach eilimint. Cinneann líon na leictreon faoisimh in adamh an cineál banna ceimiceach is féidir leis an eilimint seo a fhoirmiú. Is é an bealach is fearr le líon na leictreon faoisimh a fháil amach ná tábla tréimhsiúil na n-eilimintí a úsáid.
Chun céim
Modh 1 de 3: Cuid a hAon: Sliogáin Leictreon a Thuiscint
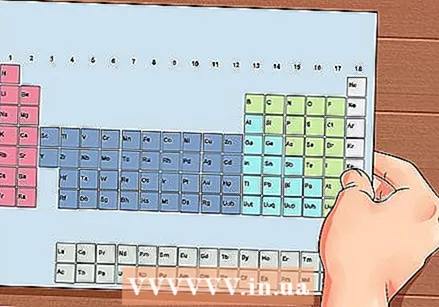 Tábla Peiriadach na nDúl. Seo tábla le cóid datha, áit a dtaispeántar eilimint i ngach cill leis an uimhir adamhach agus 1 go 3 litir mar shiombail.
Tábla Peiriadach na nDúl. Seo tábla le cóid datha, áit a dtaispeántar eilimint i ngach cill leis an uimhir adamhach agus 1 go 3 litir mar shiombail. 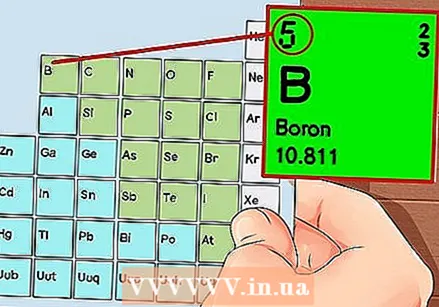 Faigh uimhir adamhach na dúile. Tá an uimhir adamhach os cionn nó in aice le siombail an eilimint. Mar shampla: Tá uimhir adamhach 5 ag Boron (B), rud a chiallaíonn go bhfuil 5 phrótón agus 5 leictreon aige.
Faigh uimhir adamhach na dúile. Tá an uimhir adamhach os cionn nó in aice le siombail an eilimint. Mar shampla: Tá uimhir adamhach 5 ag Boron (B), rud a chiallaíonn go bhfuil 5 phrótón agus 5 leictreon aige. 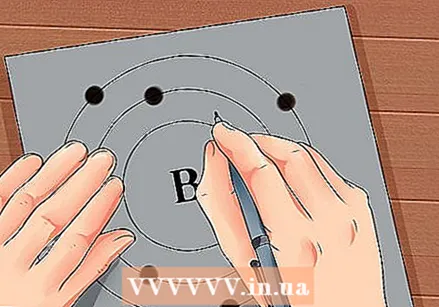 Tarraing léiriú simplí ar adamh agus cuir na leictreoin i bhfithis timpeall an núicléas. Tugtar sliogáin nó leibhéil fuinnimh ar na poist seo freisin. Socraítear an líon uasta leictreon is féidir a bheith sa bhlaosc céanna, agus líontar na sliogáin ón bhfithis istigh go dtí an fithis sheachtrach.
Tarraing léiriú simplí ar adamh agus cuir na leictreoin i bhfithis timpeall an núicléas. Tugtar sliogáin nó leibhéil fuinnimh ar na poist seo freisin. Socraítear an líon uasta leictreon is féidir a bheith sa bhlaosc céanna, agus líontar na sliogáin ón bhfithis istigh go dtí an fithis sheachtrach. - K Shell (istigh): 2 leictreon ar a mhéad.
- L Shell: uasmhéid 8 leictreon.
- M Shell: uasmhéid 18 leictreon.
- N Shell: uasmhéid 32 leictreon.
- O Shell: uasmhéid 50 leictreon.
- P Shell (seachtrach): 72 leictreon ar a mhéad.
 Faigh líon na leictreon sa bhlaosc seachtrach. Is iad seo na leictreoin faoisimh.
Faigh líon na leictreon sa bhlaosc seachtrach. Is iad seo na leictreoin faoisimh. - Nuair a bhíonn an bhlaosc faoisimh lán, tá an eilimint seasmhach.
- Mura bhfuil an bhlaosc faoisimh lán ansin tá an eilimint imoibríoch, rud a chiallaíonn gur féidir léi banna go ceimiceach le adamh eilimint eile. Roinneann gach adamh a leictreoin faoisimh mar iarracht an bhlaosc faoisimh a dhéanamh lán.
Modh 2 de 3: Cuid a Dó: Leictreoin Valence a Aimsiú i Miotail, Seachas Miotail Trasdula
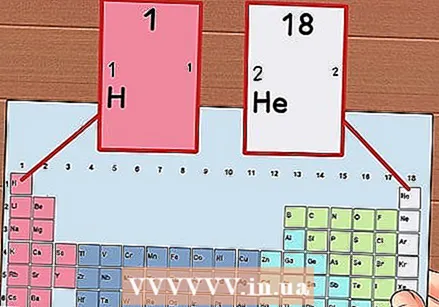 Uimhir gach colún den tábla peiriadach, ó 1 go 18. Tá hidrigin (H) ag barr cholún 1 agus Héiliam (He) ag barr cholún 18. Seo iad na grúpaí éagsúla eilimintí.
Uimhir gach colún den tábla peiriadach, ó 1 go 18. Tá hidrigin (H) ag barr cholún 1 agus Héiliam (He) ag barr cholún 18. Seo iad na grúpaí éagsúla eilimintí. 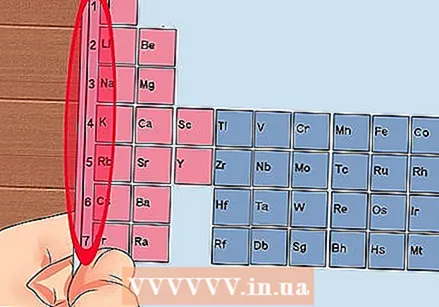 Tabhair uimhir do gach ró, ó 1 go 7. Seo tréimhsí na n-eilimintí, agus comhfhreagraíonn siad do líon na sliogán nó leibhéil fuinnimh adamh.
Tabhair uimhir do gach ró, ó 1 go 7. Seo tréimhsí na n-eilimintí, agus comhfhreagraíonn siad do líon na sliogán nó leibhéil fuinnimh adamh. - Tá 1 bhlaosc ag hidrigin (H) agus Héiliam (He), agus tá 7 ag Francium (Fr).
- Déantar na lanthanídí agus na actinides a ghrúpáil agus a liostáil faoin bpríomh tábla. Baineann gach lanthaníd le Tréimhse 6, Grúpa 3 agus baineann gach actinides le Tréimhse 7, Grúpa 3.
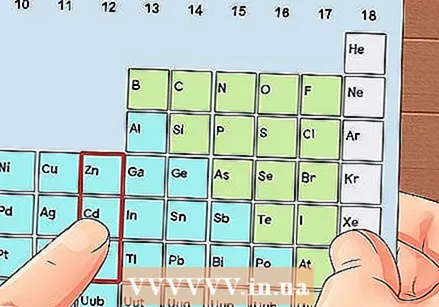 Aimsigh eilimint nach miotal trasdula í. Tá miotail trasdula i ngrúpaí 3 go 12. Léiríonn uimhreacha grúpa na miotail eile líon na leictreon faoisimh.
Aimsigh eilimint nach miotal trasdula í. Tá miotail trasdula i ngrúpaí 3 go 12. Léiríonn uimhreacha grúpa na miotail eile líon na leictreon faoisimh. - Leictreon faoisimh Ghrúpa 1: 1
- Grúpa 2: 2 leictreon faoisimh
- Grúpa 13: 3 leictreon faoisimh
- Grúpa 14: 4 leictreon faoisimh
- Grúpa 15: 5 leictreon faoisimh
- Grúpa 16: 6 leictreon faoisimh
- Grúpa 17: 7 leictreon faoisimh
- Leictreon faoisimh Ghrúpa 18: 8 - seachas Héiliam, a bhfuil 2 aige
Modh 3 de 3: Cuid a Trí: Leictreoin Valence a Aimsiú i Miotail Trasdula
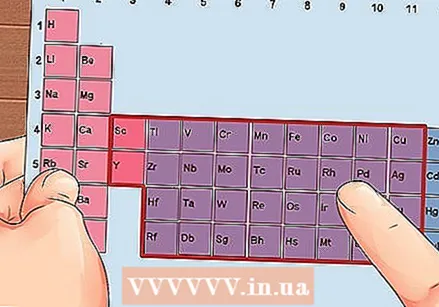 Faigh gné ó ghrúpaí 3 go 12, na miotail trasdula.
Faigh gné ó ghrúpaí 3 go 12, na miotail trasdula. Faigh líon na leictreon faoisimh bunaithe ar uimhir an ghrúpa. Freagraíonn na huimhreacha grúpa seo do líon féideartha leictreon faoisimh.
Faigh líon na leictreon faoisimh bunaithe ar uimhir an ghrúpa. Freagraíonn na huimhreacha grúpa seo do líon féideartha leictreon faoisimh. - Grúpa 3: 3 leictreon faoisimh
- Grúpa 4: 2 go 4 leictreon faoisimh
- Grúpa 5: 2 go 5 leictreon faoisimh
- Grúpa 6: 2 go 6 leictreon faoisimh
- Grúpa 7: 2 go 7 leictreon faoisimh
- Grúpa 8: 2 nó 3 leictreon faoisimh
- Grúpa 9: 2 nó 3 leictreon faoisimh
- Grúpa 10: 2 nó 3 leictreon faoisimh
- Grúpa 11: 1 nó 2 leictreon faoisimh
- Grúpa 12: 2 leictreon faoisimh
Leideanna
- Is féidir le miotail aistrithe a bheith ina sliogáin faoisimh nach bhfuil go hiomlán iomlán. Chun líon cruinn na leictreon faoisimh i miotail trasdula a chinneadh teastaíonn prionsabail áirithe teoiric chandamach atá lasmuigh de scóip an pháipéir seo.
Riachtanais
- Tábla tréimhsiúil na n-eilimintí
- Peann luaidhe
- Páipéar