Údar:
Carl Weaver
Dáta An Chruthaithe:
22 Feabhra 2021
An Dáta Nuashonraithe:
1 Iúil 2024
Ábhar
- Céimeanna
- Modh 1 de 2: Ríomh an chomhéifeacht ionsúcháin molar agus an fhoirmle á húsáid agat
- Modh 2 de 2: Aimsiú Grafach an Chomhéifeacht Ionsaithe Molar
- Earraí breise
Is éard atá sa chomhéifeacht ionsúcháin molar, ar a dtugtar comhéifeacht díothaithe molar freisin, cé chomh láidir agus a ghlacann cáithníní ceimiceacha (móilíní) substainte solas ag tonnfhad ar leith. Tá a chomhéifeacht ionsúcháin molar féin tréithrithe ag gach substaint, atá neamhspleách ar thiúchan agus toirt. Úsáidtear an tréith seo go forleathan sa cheimic agus níor cheart í a mheascadh leis an gcomhéifeacht díothaithe, a úsáidtear níos minice san fhisic. Is é an t-aonad caighdeánach tomhais le haghaidh ionsúiteacht molar ná lítear arna roinnt ar mhóil agus in aghaidh an ceintiméadar (L mol cm).
Céimeanna
Modh 1 de 2: Ríomh an chomhéifeacht ionsúcháin molar agus an fhoirmle á húsáid agat
 1 Amharc ar dhlí Bouguer-Lambert-Beer:A = ɛlc... Déantar cur síos ar ionsú solais i meán tríd an gcothromóid A = ɛlc, cá A. - an méid solais atá ag tonnfhad áirithe a ghlac an sampla isteach, ɛ - comhéifeacht ionsúcháin molar, l an fad a thaistealaíonn solas i dtuaslagán, agus c - tiúchan an tuaslagáin (líon na móilíní a ndearnadh staidéar orthu in aghaidh an aonaid aonaid).
1 Amharc ar dhlí Bouguer-Lambert-Beer:A = ɛlc... Déantar cur síos ar ionsú solais i meán tríd an gcothromóid A = ɛlc, cá A. - an méid solais atá ag tonnfhad áirithe a ghlac an sampla isteach, ɛ - comhéifeacht ionsúcháin molar, l an fad a thaistealaíonn solas i dtuaslagán, agus c - tiúchan an tuaslagáin (líon na móilíní a ndearnadh staidéar orthu in aghaidh an aonaid aonaid). - Is féidir an chomhéifeacht ionsúcháin a fháil freisin ón gcóimheas idir déine na solais a tharchuirtear tríd an gcaighdeán agus an sampla atá á staidéar. Sa chás seo, is í seo a leanas an chothromóid: A = log10(I.o/ I).
- Cinntear déine an tsolais trí speictrophotiméadar a úsáid.
- Braitheann cumas ionsúcháin tuaslagáin ar thonnfhad an tsolais a théann tríd. Ag luachanna áirithe den tonnfhad, ionsúitear solas níos láidre ná ag luachanna eile, agus braitheann na luachanna seo ar chomhdhéanamh an tuaslagáin. Agus tú ag ríomh, ná déan dearmad a chur in iúl cén tonnfhad a dhéantar iad.
 2 Tiontaigh dlí Bouguer-Lambert-Beer chun comhéifeacht ionsúcháin molar a chur in iúl. Roinn an dá thaobh den chothromóid de réir faid agus tiúchana, agus is é an toradh slonn don chomhéifeacht ionsúcháin molar: ɛ = A / lc... Agus an fhoirmle seo á húsáid agat, is féidir leat an chomhéifeacht ionsúcháin molar do thonnfhad ar leith a ríomh.
2 Tiontaigh dlí Bouguer-Lambert-Beer chun comhéifeacht ionsúcháin molar a chur in iúl. Roinn an dá thaobh den chothromóid de réir faid agus tiúchana, agus is é an toradh slonn don chomhéifeacht ionsúcháin molar: ɛ = A / lc... Agus an fhoirmle seo á húsáid agat, is féidir leat an chomhéifeacht ionsúcháin molar do thonnfhad ar leith a ríomh. - Braitheann an acmhainn ionsúcháin ag fad seasta ar thiúchan an tuaslagáin agus ar chruth an choimeádáin a úsáidtear. Cuireann comhéifeacht ionsúcháin molar deireadh leis na fachtóirí seo.
 3 Tomhais na luachanna riachtanacha ag baint úsáide as speictrophotiméadracht. I speictrophotiméadar, ritear solas le tonnfhad ar leith trí shubstaint, agus déantar déine an tsolais a tharchuirtear a thomhas ag an aschur. Glacann an tuaslagán cuid den solas agus laghdaíonn déine an tsolais. Tomhaiseann an speictrophotiméadar déine an tsolais a tharchuirtear, a úsáidtear chun comhéifeacht ionsúcháin molar a ríomh.
3 Tomhais na luachanna riachtanacha ag baint úsáide as speictrophotiméadracht. I speictrophotiméadar, ritear solas le tonnfhad ar leith trí shubstaint, agus déantar déine an tsolais a tharchuirtear a thomhas ag an aschur. Glacann an tuaslagán cuid den solas agus laghdaíonn déine an tsolais. Tomhaiseann an speictrophotiméadar déine an tsolais a tharchuirtear, a úsáidtear chun comhéifeacht ionsúcháin molar a ríomh. - Ullmhaigh tuaslagán de thiúchan aitheanta le haghaidh anailíse c... Faigh amach an tiúchan in aonaid mol / gram nó mol / lítear.
- Chun cinneadh a dhéanamh l tomhas fad an cuvette a úsáidtear. Scríobh síos an fad i gceintiméadair.
- Tomhais an ionsúiteacht le speictreafótaiméadar A. le haghaidh tonnfhad ar leith. Tomhaistear tonnfhad i méadair, ach tá an solas chomh gearr sin go gcuirtear in iúl é de ghnáth i nanaiméadar (nm). Tá an acmhainn ionsúcháin gan toise.
 4 Breiseán na huimhreacha isteach sa chothromóid agus faigh comhéifeacht ionsúcháin molar. Tóg luachanna uimhriúla A., c agus l agus breiseán iad san fhoirmle ɛ = A / lc... Iolraigh l ar an cagus ansin roinn A. faoin méid seo chun an chomhéifeacht ionsúcháin molar a fháil.
4 Breiseán na huimhreacha isteach sa chothromóid agus faigh comhéifeacht ionsúcháin molar. Tóg luachanna uimhriúla A., c agus l agus breiseán iad san fhoirmle ɛ = A / lc... Iolraigh l ar an cagus ansin roinn A. faoin méid seo chun an chomhéifeacht ionsúcháin molar a fháil. - Cuir i gcás gur thomhais tú ionsúiteacht tuaslagáin 0.05 mol / lítear ag úsáid cuvette 1 cm. Sa chás seo, ba é an ionsúiteacht 1.5 don solas le tonnfhad 280 nm. Conas an chomhéifeacht ionsúcháin molar a fháil le haghaidh tuaslagáin ar leith?
- ɛ280 = A / lc = 1.5 / (1 x 0.05) = 30 L mol cm
- Cuir i gcás gur thomhais tú ionsúiteacht tuaslagáin 0.05 mol / lítear ag úsáid cuvette 1 cm. Sa chás seo, ba é an ionsúiteacht 1.5 don solas le tonnfhad 280 nm. Conas an chomhéifeacht ionsúcháin molar a fháil le haghaidh tuaslagáin ar leith?
Modh 2 de 2: Aimsiú Grafach an Chomhéifeacht Ionsaithe Molar
 1 Tomhais déine an tsolais tarchurtha do thiúchan éagsúla an tuaslagáin. Ullmhaigh réitigh 3-4 le tiúchan éagsúla.Ag baint úsáide as speictrophotiméadar, tomhas ionsúiteacht tuaslagáin de thiúchan éagsúla do thonnfhad ar leith. Is féidir leat tosú leis an réiteach tiúchan is ísle. Níl an t-ordú tábhachtach, is é an rud is mó ná na luachanna ionsúcháin tomhaiste a mhearbhall agus a thaifeadadh de réir na dtiúchan.
1 Tomhais déine an tsolais tarchurtha do thiúchan éagsúla an tuaslagáin. Ullmhaigh réitigh 3-4 le tiúchan éagsúla.Ag baint úsáide as speictrophotiméadar, tomhas ionsúiteacht tuaslagáin de thiúchan éagsúla do thonnfhad ar leith. Is féidir leat tosú leis an réiteach tiúchan is ísle. Níl an t-ordú tábhachtach, is é an rud is mó ná na luachanna ionsúcháin tomhaiste a mhearbhall agus a thaifeadadh de réir na dtiúchan.  2 Breac na luachanna a fuarthas ar an ngraf. Breac tiúchan ar an ais-X chothrománach agus ionsúiteacht ar an ais-ingearach Y, agus breac na tomhais mar phoncanna.
2 Breac na luachanna a fuarthas ar an ngraf. Breac tiúchan ar an ais-X chothrománach agus ionsúiteacht ar an ais-ingearach Y, agus breac na tomhais mar phoncanna. - Tarraing líne idir na pointí. Má rinneadh na tomhais i gceart, ba chóir go mbeadh na pointí suite ar líne dhíreach, ós rud é, de réir dhlí Bouguer-Lambert-Beer, tá an acmhainn ionsúcháin comhréireach go díreach leis an tiúchan.
 3 Sainmhínigh fána díreachag dul trí na pointí turgnamhacha. Chun fána líne dhíreach a fháil, roinn an incrimint Y leis an incrimint X abscissa. Tóg dhá phointe ar an líne, bain na comhordanáidí comhfhreagracha pointe amháin ó chomhordanáidí an phointe eile, agus roinn an difríocht Y leis an difríocht X.
3 Sainmhínigh fána díreachag dul trí na pointí turgnamhacha. Chun fána líne dhíreach a fháil, roinn an incrimint Y leis an incrimint X abscissa. Tóg dhá phointe ar an líne, bain na comhordanáidí comhfhreagracha pointe amháin ó chomhordanáidí an phointe eile, agus roinn an difríocht Y leis an difríocht X. - Faightear fána líne dhíreach (fána, nó tadhlaí na fána) mar a leanas: (Y.2 - Y.1) / (X.2 - X.1). Sa chás seo, tugtar innéacs 2, agus an pointe íochtarach - an t-innéacs 1 don phointe atá suite níos airde feadh na líne dírí.
- Cuir i gcás, ag tiúchan molar de 0.2, go raibh an ionsúiteacht 0.27, agus ag tiúchan 0.3, bhí sé 0.41. Déantar ionsú a bhreacadh ar an ais-Y agus an tiúchan ar an ais-X. Agus an chothromóid thuas á úsáid agat, faigh fána líne dhíreach: (Y2 - Y.1) / (X.2 - X.1) = (0,41-0,27)/(0,3-0,2) = 0,14/0,1 = 1,4.
 4 Chun comhéifeacht ionsúcháin molar a fháil, roinn fána líne dhíreach leis an gcosán a thaistil an solas (doimhneacht an cuvette). Is ionann an cosán a thaistil an solas agus doimhneacht an chuvette a úsáidtear sa speictrophotiméadar.
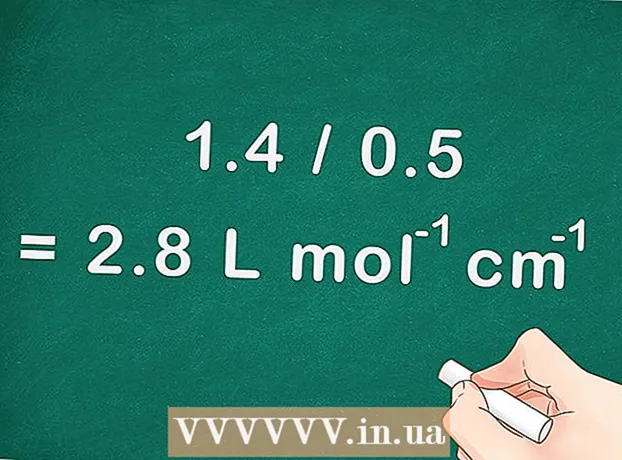
4 Chun comhéifeacht ionsúcháin molar a fháil, roinn fána líne dhíreach leis an gcosán a thaistil an solas (doimhneacht an cuvette). Is ionann an cosán a thaistil an solas agus doimhneacht an chuvette a úsáidtear sa speictrophotiméadar. - Mar shampla, faighimid: má tá an fána 1.4, agus doimhneacht an cuvette 0.5 ceintiméadar, ansin is é comhéifeacht ionsúcháin molar 1.4 / 0.5 = 2.8 L mol cm.
Earraí breise
 Conas méadair chearnacha a ríomh
Conas méadair chearnacha a ríomh  Conas líon na bprótón, na neodrón agus na leictreon a fháil
Conas líon na bprótón, na neodrón agus na leictreon a fháil  Conas leictreoin faoisimh a chinneadh
Conas leictreoin faoisimh a chinneadh  Conas cothromóidí ceimiceacha a chothromú
Conas cothromóidí ceimiceacha a chothromú  Conas cumraíocht leictreonach adamh aon eilimint a scríobh
Conas cumraíocht leictreonach adamh aon eilimint a scríobh  Conas tiúchan tuaslagáin a ríomh
Conas tiúchan tuaslagáin a ríomh  Conas polaraíocht tuaslagáin a ríomh
Conas polaraíocht tuaslagáin a ríomh  Conas líon na neodrón in adamh a fháil
Conas líon na neodrón in adamh a fháil  Conas uisce óil a dhéanamh as salann
Conas uisce óil a dhéanamh as salann  Conas an tábla peiriadach a úsáid
Conas an tábla peiriadach a úsáid  Conas oighear tirim a stóráil
Conas oighear tirim a stóráil  Conas oighear tirim a dhéanamh
Conas oighear tirim a dhéanamh  Conas taos fiacla eilifint a dhéanamh
Conas taos fiacla eilifint a dhéanamh  Conas an tuaslagán a chaolú
Conas an tuaslagán a chaolú